부작용 적고 시술성공률 높은 차세대 항암치료 기대
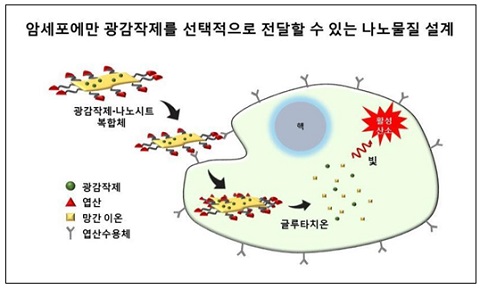
1) 암세포에 과다 발현돼 있는 엽산 수용체에 특이적으로 결합해 암세포만 선택적으로 인식할 수 있는 기능성 나노시트 개발
2) 광감작제-나노시트 복합체는 암세포 내 다량 존재하는 글루타치온에 의해 나노시트가 분해돼 적재된 광감작제가 방출된다.
3) 조사된 빛에 의해 활성산소를 발생시켜 암세포를 효과적으로 사멸시킨다.
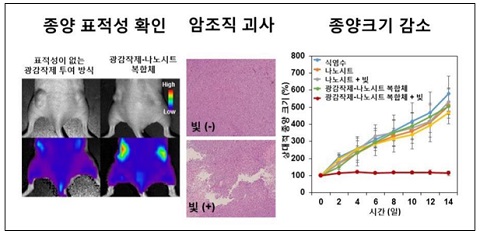
전신에 투여해 준 광감작제-나노시트 복합체가 종양 특이적으로 축적되는 것을 형광 이미징을 통해 확인(왼쪽)
조직병리 검사를 통해 선택적 암세포 사멸 확인(가운데)
빛 조사 후 2주간 관찰한 결과, 광감작제-나노시트 복합체를 투여해 준 생쥐에서 종양성장이 효과적으로 억제됨(오른쪽)
2차원 광감작제-나노시트 복합체는 암세포만을 선택적으로 없애기 때문에 정상 조직의 손상을 최소화할 수 있으며, 기존 광역동 치료에 비해 난용성 광감작제 투여량을 1/10로 줄여도 치료효과를 갖는다. 또한 암세포 치료 후 복합체가 체내에서 분해되기 때문에 독성이 적다. 개발한 복합체의 치료효과를 동물 실험을 통해 확인했고, 광역동 치료에 적용이 기대된다.
기존의 반복적인 항암제 투여와 방사선 치료법 등의 항암치료는 경제적 부담과 많은 전신 부작용을 야기하는 단점이 있다. 광역동치료는 기존 항암치료와 달리 인체에 무해한 빛을 사용해 국소적인 암세포 치료가 가능하므로 정상 세포의 손상을 최소화하기 때문에 암치료의 새로운 대안으로 부각되고 있다.
광역동치료는 광감작제가 특정 파장대의 빛을 흡수해 에너지전달 기작을 거쳐 활성산소를 내어 주변의 암조직을 손상시켜 치료하는 방법이다.
그러나 광역동치료에 사용되는 핵심 물질인 광감작제는 대부분 물에 잘 녹지 않으며, 투여된 광감작제가 정상 조직에도 남기 때문에 햇볕을 쬐면 체내에 잔존한 광감작제에 의해 발생하는 활성산소가 피부를 심각하게 손상시키는 등 부작용을 유발한다.
따라서 난용성 광감작제의 적용 한계를 극복하고, 최소한의 광감작제를 전신투여해 암세포만 선택적으로 사멸시켜 부작용을 줄일 수 있는 새로운 광역동 치료법이 필요하다.
연구팀은 기존 광역동치료의 한계를 극복하기 위해 혈액 내 안정성이 높고 암세포 내 환경에서는 쉽게 분해되는 이산화망간 나노시트에 주목해, 암세포에만 선택적으로 광감작제를 전달할 수 있는 기능성 나노시트를 개발했다.
많은 암세포에는 엽산 수용체가 과다 발현돼 있기 때문에, 엽산을 도포한 나노시트를 사용하면 선택적으로 암세포에만 나노시트가 전달되고 축적이 가능하다는 아이디어를 기반으로 엽산이 도포된 이산화망간 나노시트를 합성했다.
넓은 표면적을 가진 시트 표면에 난용성 광감작제를 효과적으로 적재하고, 체내 투여 시 혈액 내에서 분해나 분리되지 않고 안정성을 유지해 무분별한 광감작제의 방출을 억제하며, 일단 암세포 내로 들어간 나노시트는 암세포 내에 높은 농도로 존재하는 글루타치온(Glutathione, GSH)에 의해 완벽하게 분해되면서 적재된 광감작제가 방출되는 것을 종양 동물 모델을 통해 확인했다.
생쥐 실험에서 기존의 광감작제 투여량 대비 10%만 혈관 투여해도 뛰어난 항암효과를 보였으며, 암세포 표적 광역동치료 효과를 획기적으로 개선했다.
민달희 교수는 “이 연구는 정상세포의 손상을 최소화하면서 암세포만을 표적 치료하는 생체적합적인 2차원 나노시트를 개발한 것이다. 폐암, 식도암, 자궁경부암 등 다양한 난치성 암 치료에 적용할 수 있을 것이다. 부작용이 적고 시술성공률이 높은 차세대 항암치료 기술로 발전시키는 데 기여할 것으로 기대된다”고 연구 의의를 설명했다.
민달희 교수 연구팀의 연구는 응용화학 분야 국제학술지인 투디 머티리얼즈(2D Materials) 4월 11자에 ‘Functional Manganese Dioxide Nanosheet for Targeted Photodynamic Therapy and Bioimaging In Vitro and In Vivo’, 민달희 교수(교신저자, 서울대, ㈜레모넥스 최고책임기술이사), 김성찬 연구원(제1저자, 서울대), 안성민 연구원(공저자, 서울대), 이지선 연구원(공저자, 서울대), 김태식 연구원(공저자, 서울대) 등으로 게재됐다.

