생명현상 물리화학적 연구의 새 패러다임 제시
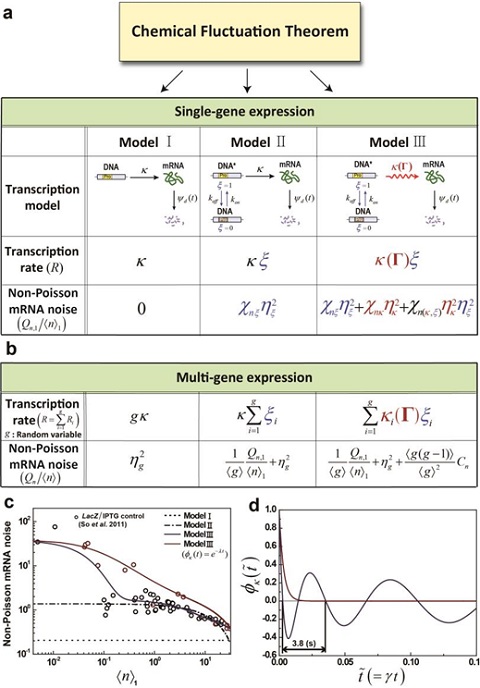
(a) 단일유전자 전사모델. Model I에서는 전사반응 속도가 상수이며, DNA 상태는 1개만 존재한다. Model II에서는 DNA 상태는 2개가 존재하고, 전사반응 속도는 상수로 취급되고 있다. Model III는 세포상태변수에 의존하는 전사반응 속도를 도입한 본 연구에서 제시하는 새로운 모델이다. 각 모델에 대해 화학반응요동법칙을 이용해 얻은 mRNA 요동의 해석적 표현
(b) 유전자가 여러 개일 경우에 각각의 전사반응 Model에 관한 Non-Poisson mRNA 요동에 대한 해석적 표현
(c) 대장균의 lacZ 유전자에서 발현되는 mRNA의 개수 조절능력 실험 결과 해석. Model III의 경우, 청색선은 정상 생장조건, 적색선은 세포성장속도가 느린 경우를 나타낸다.
(d) Model III의 해석을 통해 얻어진 전사반응속도의 시간 상관함수. 이 생장조건에 따른 시간 상관함수 변화는 활성 유전자 전사과정 메카니즘과 동력학을 사용하여 설명할 수 있다.
Non-Poisson mRNA 요동 : mRNA 개수분포의 분산에서 평균을 뺀 양을 평균의 제곱으로 나눈 양
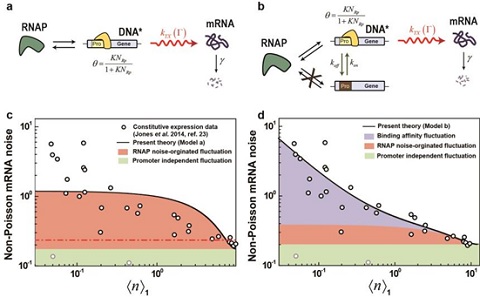
(a,b) DNA로부터 mRNA를 합성해 내는 효소인 RNA 중합효소와 이 효소가 DNA에 붙는 자리인 프로모터 사이의 결합세기가 변하지 않는 경우와 DNA 구조 변화에 따라 요동치는 경우에 해당하는 각각의 전사 모델
(c,d) 모델 a와 b를 통한 mRNA의 농도 요동 실험결과에 대한 정량분석. 전사 초기 단계에서 RNA 중합효소와 프로모터 사이의 결합세기의 요동이 mRNA 개수 통계에 있어 중요한 역할을 함을 보여준다.
한국연구재단(이사장 조무제)은 성재영 교수(중앙대, 세포화학동력학 연구단)가 윤상운 교수(중앙대), 김지현 교수(중앙대), 필립 김 교수(토론토대학)와의 공동연구를 통해 세포 내에서 생성되고 소멸되는 분자들의 농도 요동을 지배하는 법칙인 ‘화학요동법칙‘을 발견했다고 밝혔다.
모든 생명 기능들은 세포 내 유전자에 저장된 정보를 mRNA와 단백질로 발현하고 이들을 소멸시키는 화학반응들을 통해 구현된다. 이 화학반응들이 근본적으로 불확실성을 내재한 확률 과정이기 때문에 똑같은 유전자를 가진 세포들도 mRNA와 단백질 농도가 세포마다 크게 달라 세포의 성질과 기능이 다양할 수 있다는 것은 알려진 사실이다.
하지만 이 현상을 물리화학적 모델로 설명하거나 예측하는 것은 불가능에 가까운 것으로 여겨져 왔다. 그 이유는 유전자 발현 과정을 구성하는 화학반응 과정들이 기존 모델이나 이론들이 가정하는 것보다 훨씬 복잡한 확률 과정이기 때문이다.
연구팀은 이 난제를 해결하기 위해 아무리 복잡한 확률 과정을 거쳐 생성 및 소멸되는 분자들에 대해서도 그 농도의 요동이 따르게 되는 ‘화학요동법칙’을 수학적 연역을 통해 최초로 발견했다. 이 결과를 유전자 발현 과정에 적용해 유전자가 같은 세포들의 mRNA 및 단백질 개수 조절 능력이 유전자 종류나 화학적 환경변화에 따라 변화하는 정도를 측정한 다양한 실험 결과들을 일관되게 설명하고, 이 과정에서 유전자 발현 과정에 대한 새로운 물리화학적 모델을 구축하는 데 성공했다.
이 연구 결과는 지난 백년간 널리 받아들여진 반트호프의 화학반응 속도론과 파울리의 마스터 방정식 접근법의 기본 가정들이 세포 내 화학 반응에 대해서는 성립하지 않는다는 것을 선명하게 보여주고 이 문제에 대한 해결책을 제시하는 것이다.
연구팀은 더 나아가 화학요동법칙을 사용해 세포 내 mRNA 소멸 과정 기작에 따라 세포의 mRNA 농도 조절 능력이 변화하는 것을 예측하고, 이 예측이 정확한 전산모사 결과와 일치함도 보여 주었다. 살아 있는 세포 실험 결과에 대한 이와 같은 정량적 설명과 예측은 과학 사상 전례가 없는 성과이다.
성재영 교수는 “이 연구는 생명현상을 수학적 연역과 물리화학적 모델을 사용해 정량적으로 설명‧예측하는 새로운 연구 패러다임을 제시한 것”으로 학문적 의미를 부여하며, ”이 새로운 방향의 연구가 생명체들이 어떤 방식으로 얼마나 정확하게 다양한 생명 기능들을 구현하고 조절하는지를 물리화학적으로 이해하고, 세포의 생명기능 조절 능력을 회복시켜 질병을 치료하는 새로운 의학적 방법을 제시하는 데 기여할 수 있을 것“으로 전망했다.
이 연구는 한국연구재단 리더연구자지원사업의 지원으로 수행됐다. 연구 성과는 순수이론 논문으로서는 매우 이례적으로 네이쳐 저널 그룹의 네이쳐 커뮤니케이션즈(Nature Communications)에 논문명 ‘The Chemical Fluctuation Theorem governing gene expression’, 박성준 박사(제1저자, 중앙대학교), 송상근(공동저자, 중앙대학교), 양길석(공동저자, 미국 코넬대학교), 필립 김 교수(Philip M. Kim, 공동저자, 캐나다 토론토대학교), 윤상운 교수(교신저자, 중앙대학교), 김지현 교수(교신저자, 중앙대학교), 성재영 교수(교신저자, 중앙대학교) 등으로 1월 19일에 게재됐다.

