유전자 서열 분석으로 맞춤형 면역항암치료 가능성 열려
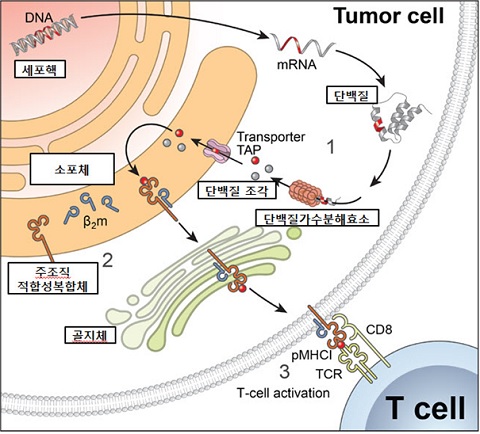
① 변형된 DNA(왼쪽 위)는 변형된 단백질을 생성한다(오른쪽 위).
② 변형된 단백질은 단백질가수분해효소에 의해 분해되고 이 때 생성된 짧은 길이의 단백질 조각은 주조직 적합성 복합체와 결합해 암 세포 바깥으로 표지된다.
③ 이후 T-세포와 같은 면역세포에 의해 감지된 후 면역반응이 활성화된다(오른쪽 아래).
한국연구재단(이사장 조무제)은 연세대학교 김상우 교수 연구팀이 차세대 염기서열법으로 암 특이적 항원을 정확히 찾아내는 기술을 개발했다고 밝혔다.
정상 세포가 암세포로 변하면 원래 세포에 없던 단백질이 만들어지고 그 일부는 면역반응을 일으키는 ‘신항원(neoantigen)’이 된다. 면역항암치료는 수지상세포, 자연살해세포, T-세포와 같은 면역세포를 암세포의 신항원에 반응하게 해 암을 죽이는 방법이다.
면역항암치료는 기존 항암제와 달리 암의 종류에 구애받지 않고 부작용이 거의 없는 장점이 있다. 하지만 항원을 정확하게 찾아내기 힘들어 전체 환자의 약 20% 정도에서만 효과를 보인다. 항원 분류의 정확도를 높여야 환자의 암세포에 특이적인 항원을 찾아 효과적인 백신을 만들 수 있다.
연구팀은 개인의 유전자 서열 정보를 값싸고 빠르게 알아내는 차세대 염기서열법으로 신항원의 생성 여부를 판단하는 프로그램을 개발하고 이를 ‘네오펩시(Neopepsee)’라고 명명했다.
암세포는 정상세포보다 DNA 변이가 훨씬 많이 생기는데, 네오펩시는 누적된 DNA 변이로 인해서 만들어진 변형 단백질의 종류를 분석해 낸다. 단백질의 서열, 크기, 전하량 등 아홉 개의 분자 특성을 이용해 면역반응을 일으키는지 여부를 판단한다.
변형 단백질과 세포 내 단백질(주조직적합성복합체)의 결합성만을 활용하는 기존 방법에 비해, 네오펩시는 더 많은 단백질 특성을 활용하므로 정확성이 높다. 피부암의 일종인 흑색종을 대상으로 네오펩시를 활용했을 때 최대 3배의 정밀도를 보였다.
네오펩시는 기계학습법(machine learning)을 기반으로 약 1만5천건의 데이터를 학습해 면역반응을 판단하도록 설계됐다.
또한 연구팀은 암세포 내 변형 단백질 서열이 세균, 바이러스 등에 존재하는 항원과 비슷할수록 면역반응을 잘 일으킨다는 사실도 추가적으로 밝혀냈다.
김상우 교수는 “네오펩시는 환자가 갖고 있는 유전자 돌연변이만으로 면역항암치료 효과를 예측할 수 있고, 또한 효과를 대폭 향상시킬 수 있다”고 설명했다.
이 연구는 과학기술정보통신부·한국연구재단 기초연구사업(신진연구자)의 지원으로 수행됐으며, 의약학 분야 국제학술지 종양학 연보(Annals of Oncology) 1월 19일에 논문명 ‘Neopepsee : accurate genome-level prediction of neoantigens by harnessing sequence and amino acid immunogenicity information’, 김상우 교수(교신저자, 연세대학교 의과대학 의생명과학부), 김소라 박사과정생(공동 제1저자, 연세대학교 의과대학 의생명과학부), 김한상 박사과정생/전문의(공동 제1저자, 연세대학교 의과대학 약리학교실), 김은영 박사과정생(연세대학교 의과대학 의생명과학부), 이민구 교수(연세대학교 의과대학 약리학교실), 신의철 교수(KAIST 의과학대학원), 백순명 교수(연세대학교 의과대학 의생명과학부) 등으로 게재됐다.

