항생제 비의존적 감염 치료 및 보조제 개발 가능성 커져
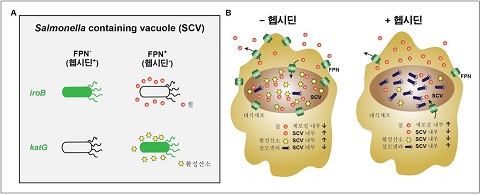
헵시딘에 의해 대식세포 내의 철의 양이 조절됨으로써 실제로 숙주의 방어기작 중 하나인 활성산소(ROS) 생성에 영향을 주어 숙주/병원체 간 생존에 영향을 주게 된다.
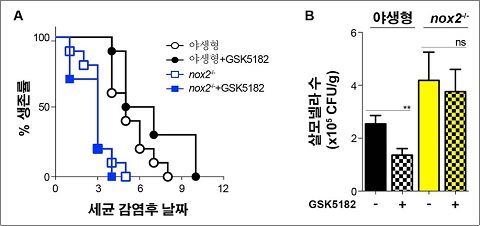
헵시딘 발현 억제제(GSK5182)를 투입하면 숙주 내부의 철의 양이 증가하며 숙주의 생존 능력이 증가한다. 뿐만 아니라 박테리아의 수도 줄어든다. 이로써 세균감염에 대한 방어기작이 철 대사에 따라 달라짐을 알 수 있다.
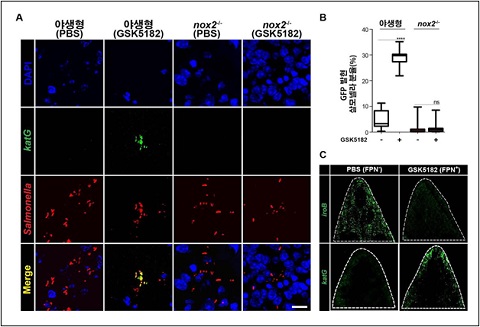
숙주 내 철 농도 변화를 통한 살모넬라의 반응을 확인하기 위해, 헵시딘 발현 억제제(GSK5182)를 처리해 살피고 대식세포에서의 방어기작인 활성산소(ROS)는 ROS 바이오센서를 이용해 관찰했다.
헵시딘 발현 억제(GSK5182+)로 인해 철 농도가 많을 때(iron+), 활성산소(ROS) 생성은 증가하고, 이에 따라 살모넬라의 katG 유전자 발현(ROS 바이오센서)이 증가한다.활성산소 증가는 대식세포 내의 살모넬라가 감소되도록 유도하고, 이는 숙주의 생존에 유리하다.
한국연구재단은 전남대학교 최현일 교수 연구팀이 식중독 균인 살모넬라에 감염됐을 때 철 농도 조절을 통한 감염 억제 방법을 규명했다고 밝혔다.
우리 몸의 철 항상성은 헵시딘이라는 호르몬에 의해 조절된다. 헵시딘은 세포막의 단백질인 FPN1을 통해 세포 내외의 철 농도를 조절하는 것으로 알려져 있다.
연구팀은 살모넬라가 증식하는 장소인 대식세포 내 소기관(SCV)에도 헵시딘이 작용해 철 농도가 조절된다는 것을 규명했다. 또한, 헵시딘에 의한 철 대사 조절은 항균작용을 하는 활성산소(ROS)의 생성과 연관이 있음을 밝혀냈다..
헵시딘에 의해 SCV 안의 철 농도가 감소하면 대식세포에서 활성산소(ROS) 생성이 저해된다. 그 결과 살모넬라가 활발히 증식할 수 있다. 반대로 동물 감염 실험에서 헵시딘 발현 억제제인 GSK5182를 처치하면 활성산소가 증가돼 살모넬라를 효과적으로 사멸시켰다.
최현일 교수는 “이 연구는 병원균과 숙주 모두에게 중요한 핵심 공유인자로서의 철 성분의 중요성을 발굴해, 세균감염에 대한 새로운 이론을 제시한 것”이라며, “이를 바탕으로 신개념 비항생제성 감염치료제 및 치료보조제가 개발될 것으로 기대된다”고 연구의 의의를 설명했다.
이 연구는 과학기술정보통신부·한국연구재단 기초연구사업(중견연구)의 지원으로 수행됐으며, 국제학술지 네이처 커뮤니케이션즈(Nature Communications) 5월 29일에 논문명 ‘The hepcidin-ferroportin axis controls the iron content of Salmonella-containing vacuoles in macrophages’, 최현일 교수(교신저자, 전남대학교), 임대진(공동제1저자, 전남대학교), 정재호(공동제1저자, 전남대학교), 김광수(공동제1저자, 전남대학교) 등으로 게재됐다.

