몸 속 단백질을 매개로 종양에만 전달되는 암 치료제
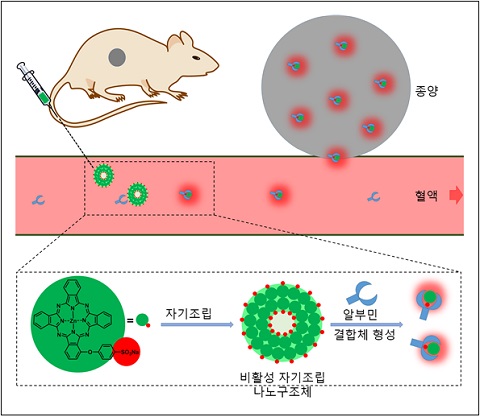
NanoPcS가 자발적으로 조립된 구조를 이루고 비활성화(off)돼 있다. 그러나 이 구조가 해체되면서 알부민과 결합하면 활성화(on)돼 종양조직으로 전달되고, 생체 내 형광 이미징 및 종양 치료 효과를 보인다.
윤주영 교수(이화여대), 남기택 교수(연세대), 최선 교수(이화여대) 공동 연구팀이 기존의 복잡한 나노시스템을 벗어나 단일 분자만으로 광역학 암 치료와 이미징이 가능한 방법을 개발했다고 한국연구재단(이사장 노정혜)이 밝혔다.
테라노스틱스는 치료(therapy)와 진단(diagnostics)이 동시에 이루어진다는 뜻의 합성어이다. 암 부위를 표적으로 하는 물질을 이용해 암을 진단하는 동시에 병변 부위에만 치료제를 전달할 수 있는 맞춤의학의 일환이다.
최근까지 특정 단백질 인식, 소수성 리간드 결합 등을 이용한 방법이 보고됐으나 대부분 많은 구성요소가 필요하고 제조 단계가 복잡하다는 한계가 있다.
연구팀은 표적 인식, 치료 효능, 형광 이미징 등 다양한 기능을 동시에 해내는 단일 분자 형태(one for all)의 치료제를 개발했다. 기존 시스템의 단점을 극복하고 우수한 종양 표적화 능력과 광역학 치료 효과를 입증했다.
개발된 치료제는 광역학 치료 효능을 가진 프탈로사이아닌 유도체를 기반으로 한다. 이 물질은 알부민 단백질과 결합해 종양 조직에만 선택적으로 전달된다. 그 다음 레이저가 조사되면 활성산소 종을 생성해 종양을 치료한다. 또한 이 물질은 형광 이미징이 가능하므로 치료제를 추적하고 모니터링할 수 있다.
연구팀이 간암 및 자궁암 유발 생쥐에서 개발된 치료제를 주입한 후 레이저를 조사한 결과, 6주 이후 암 치료효과가 나타났고 20주까지 효과가 지속됐다.
연구팀은 “광역학 치료제가 생체 내 존재하는 혈청 알부민 단백질과 결합해 종양으로 선택적으로 전달되는 직접적인 연구결과”라고 연구의 의의를 설명하며, ”향후 투여된 나노물질의 체내 장기 전달 효율을 높여 치료효과를 증가시키는 연구를 지속하겠다”고 밝혔다.
이 연구 성과는 과학기술정보통신부·한국연구재단 기초연구사업(리더연구, 선도연구센터), 바이오·의료기술개발사업사업의 지원으로 수행됐다.
국제학술지 ‘미국화학회지(Journal of the American Chemical Society)’에 12월 20일, 논문명 ‘In Vivo Albumin Traps Photosensitizer Monomers from Self-Assembled Phthalocyanine Nanovesicles : A Facile and Switchable Theranostic Approach’, 윤주영 교수(교신저자, 이화여대), 남기택 교수(교신저자, 연세대), 최선 교수(교신저자, 이화여대), 황지안동(Huang Jian-Dong) 교수(교신저자, 푸저우대학교), 리싱슈(Li Xingshu)(제1저자, 이화여대), 유성숙(연세대), 이윤지(연세대), 거티안(Guo Tian)(푸저우대학교), 권나현(이화여대), 이다영(이화여대), 염수정(서울대), 조예진(연세대), 김경미(이화여대) 등으로 게재됐으며 표지논문으로 출간될 예정이다.

