신경세포 내 비정상적 침착물 형성을 저해하는 ARSA의 분자샤프론 기능 규명
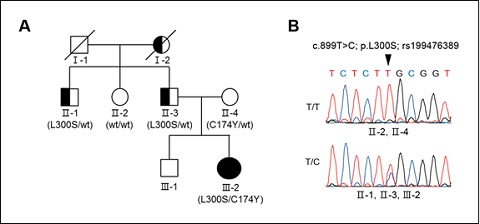
파킨슨병 환자인 II-1과 II-3에서 ARSA 유전자 내의 돌연변이를 확인했다.
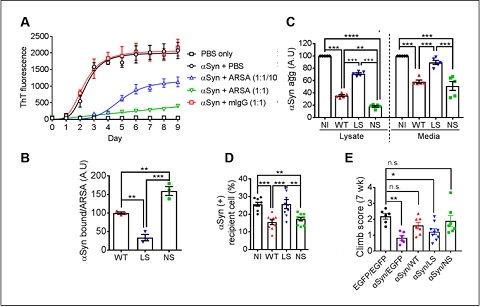
알파-시뉴클린의 응집화 과정이 ARSA 농도에 의존적으로 감소함(그림 A).
ARSA는 알파-시뉴클린과 결합하며(그림 B), 세포에 발현시 알파-시뉴클린 응집체의 형성, 세포밖 분비, 세포간 전이를 감소시킴(그림 C, D).
파킨슨병 환자에서 관찰되는 돌연변이 ARSA의 경우, 알파-시뉴클린과의 결합이 약하고, 효과적으로 응집체를 감소시키지 못했다.
이상의 결과는 알파-시뉴클린 발현에 의한 초파리 모델의 운동능력 분석에서도 검증됐다(그림 E).
한국연구재단(이사장 노정혜)은 이승재 교수(서울대)·이준성 박사 연구팀이 공동연구(일본 준텐도대학 하토리 교수, 호주 시드니대학 할리데이 교수, 일본 오사카대학 나가이 교수, 연세대 이필휴 교수)를 통해 파킨슨병 발병과 진행을 조절하는 새로운 인자를 발굴, 진단을 위한 마커 및 치료제 개발의 실마리가 될 것으로 기대된다고 밝혔다.
파킨슨병 환자의 신경세포에서 나타나는 비정상적 침착물의 주요 성분과 결합해 침착물 형성을 억제할 수 있는 단백질(ARSA, aryl sulfatase A)을 규명한 것이다.
파킨슨병은 비정상적 단백질 응집체가 신경세포에 축적되고 인접 세포로 전이되는 병리현상이 잘 알려져 있으나 이 응집체가 어떻게 형성되고 분해되는지 상세한 조절기전은 밝혀지지 않았다.
한편, 세포 안에는 역할을 다한 단백질 등을 분해해 처리하는 폐기물 처리 기구 리소좀이 존재해 리소좀 가수분해효소와 파킨슨병과의 연관성에 대한 관심이 이어지고 있었다.
연구팀은 리소좀 가수분해효소 ARSA 유전자에 돌연변이가 있는 희귀유전질환 가계 내 파킨슨병 환자가 있는 점에 주목했다.
또한, 다른 파킨슨병 환자들의 혈액샘플에서 ARSA 단백질 농도를 분석해 본 결과 인지수행 능력이 좋을수록 ARSA 단백질 농도가 높아지는 비례 경향을 확인했다.
유전자 및 혈액 분석을 토대로 연구팀은 ARSA와 파킨슨병과의 연관성에 주목하고 나아가 세포 및 동물모델 연구를 통해 ARSA가 단백질 침착물의 주요 성분인 알파-시뉴클린과 직접 결합, 침착물 형성을 방해하는 것을 알아냈다.
ARSA는 리소좀에 존재하며 세포막 분해산물인 설파티드(sulfatide)를 분해하는 가수분해효소로 리소좀 축적질환(이염성 백질영양장애)의 원인 유전자로 주로 알려져 있었다.
하지만 이번 연구로 가수분해효소 역할과 별개로 ARSA가 세포질에도 존재하며 단백질이 제 역할을 하도록 입체구조를 갖추는 과정에서 응집되지 않도록 돕는 분자샤프론으로 기능함을 알아냈다.
단백질은 리보솜에서 여러 아미노산들이 연결된 끈 상태로 처음 생성되는데 생명을 지탱하는 기능분자로 작용하기 위해서는 접힘(foling) 과정 등을 통해 적절한 형태(입체구조)를 갖추어야 하며, 단백질이 생성되고 분해되기까지 적절한 구조를 형성하도록 돕는 데 관여하는 단백질들을 분자샤프론(molecular chaperone)이라고 지칭한다.
실제 예쁜꼬마선충(C.elegans) 모델을 통해 ARSA 유전자에 결함이 있을 경우 신경근연접에서 알파-시뉴클린 응집체가 형성되고 인접 세포로 전이되는 현상이 증가하는 것을 확인했다.
마찬가지로 파킨슨병 모델의 초파리에서 ARSA 유전자를 도입한 결과 운동능력의 감소가 완화되는 것을 확인했다.
파킨슨병 환자에서 발견됐던 돌연변이 ARSA는 알파-시뉴클린과의 결합력이 약하고 응집체 형성을 효율적으로 억제하지 못하는 것을 밝힌 이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 중견연구사업, 선도연구센터사업 등의 지원으로 수행됐고, 국제학술지 브레인(Brain)에 9월 1일 논문명 ‘Arylsulfatase A, a genetic modifier of Parkinson’s disease, is an α-synuclein chaperone’, 이승재 교수(교신저자/서울대학교), 이준성 박사(제1저자/당시 소속 서울대학교) 등으로 게재(프린트판)됐다.

