유럽 규정 강화(CE-MDR)에 따라 5개 업체에 각각 2,000만원 지원
보건복지부는 유럽 인허가 제도 강화에 따라 국내 의료기기 기업의 해외시장 진출을 돕기 위해 진단용 엑스선 촬영 장치를 포함한 총 5개 기업 제품을 지원한다고 밝혔다.
최근 의료기기와 관련해 전세계적으로 유효성 및 안전성에 대한 인식이 높아지고 있으며, 특히 유럽에서는 5월부터 강화된 인허가 규정을 적용하기로 발표한 상황이다.
새로운 유럽 인증 규정(MDR)은 임상 자료 요건 강화 및 시판 후 감시활동 강화 등을 핵심 내용으로 한다.
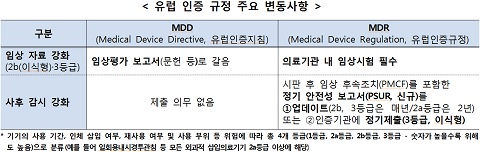
이러한 변화로 인해 임상평가보고서 등 문서작성 및 인증 심사 비용 부담이 증가해 국내 중소 의료기기 기업이 인허가를 갱신하는 데 어려움을 겪을 것으로 예상된다.
특히 국내 의료기기 기업들은 유럽 인증을 활용해 신남방 국가 및 중동에도 진출하고 있기 때문에 이에 대한 준비가 중요하다.
이번에 선정된 5개 기업은 유럽 기준 2a등급 이상인 제품을 제조하고 있으며, 수출 비중이 높아 유럽 인증 강화에 선제적으로 대응할 필요성이 높은 상황이다.
보건복지부에서는 선정된 이들 기업과 전문 상담(컨설팅) 기업으로 구성된 연합체(컨소시엄)에 개소당 2,000만 원을 지원하며, 최종 유럽 인증을 획득하기까지 지속 관리할 예정이다.
한편, 올해 하반기에는 전체 의료기기 기업을 대상으로 새로운 유럽 인증 규정에 대한 정보 제공 세미나를 개최하고 규제준수책임자 전문성 유지·향상 활동을 위한 교육도 할 계획이다.
보건복지부 임인택 보건산업정책국장은 “최근 진단키트 등으로 국산 의료기기에 대한 해외 수요가 높은 상황에서 외국 제도 변화에 선제 대응해 국내 의료기기 기업의 수출 및 국제 경쟁력을 지속적으로 확보할 수 있도록 하겠다”고 밝혔다.

